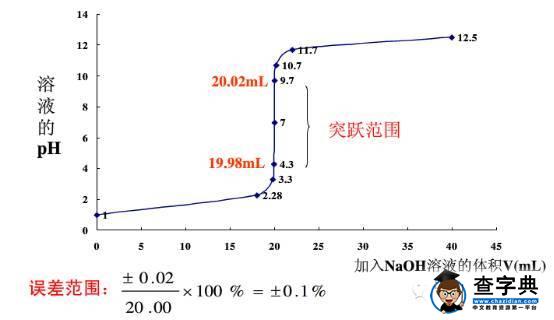
滴定实验酸碱指示剂的选择
指示剂选取的原则:一般要求指示剂颜色变化明显,变色pH范围窄,指示准确。
石蕊因变色pH(5-8)范围宽及人的肉眼对红—紫—蓝的颜色变化不敏感,一般不作滴定指示剂。
强酸与强碱间的相互滴定,生成的盐不水解,溶液显中性,选择甲基橙或酚酞均可。
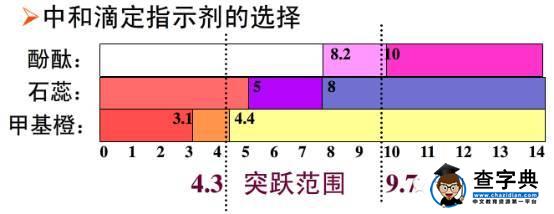
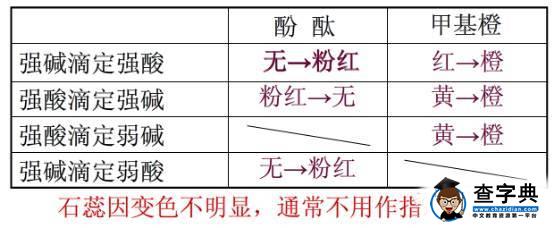
酚酞:
酸滴定碱——颜色由红色刚好褪色
碱滴定酸——颜色由无色到浅红色
甲基橙:
酸滴定碱——颜色由黄色到橙色
碱滴定酸——颜色由红色到橙色
强酸与弱碱及强碱与弱酸之间的滴定要求指示剂变色的pH范围尽可能与生成盐的水解得到溶液的pH吻合,以保证中和反应完全,指示剂指示准确。故一般强碱滴弱酸选择酚酞(生成强碱弱酸盐水解使溶液显碱性),强酸滴弱碱选择甲基橙(生成强酸弱碱盐水解使溶液显酸性)。
问题1、如果做酸碱中和滴定实验(用0.1mol/L的盐酸溶液滴定已知浓度为0.1mol/L体积为20mL的氢氧化钠溶液,假如滴定时所用盐酸体积为VmL。)选用甲基橙作指示剂,滴定终点溶液由黄色变为橙色,因为甲基橙的变色范围pH为3.1—4.4之间(其中处于3.1—4.4之间为橙色),显然当甲基橙变色时,pH肯定比7要小的多,是不是可以说明选甲基橙作指示剂比选酚酞作指示剂误差要大的多?

问题2、用酚酞作指示剂,滴定终点时,溶液由粉红色变为无色,显然此时溶液的pH值只要小于8均为无色,也就是说pH值并不一定等于7,我感觉指示剂的挑选有问题?